Comprar planes
Comprar tu propia cobertura
Planes a través de tu empleador
Conoce sobre los beneficios médicos, dentales, de farmacia y voluntarios que tu empleador puede ofrecer.
Aprender
¿Vives o trabajas fuera del país?
Síndrome de Birt-Hogg-Dubé (PDQ®) información para profesionales de salud [NCI]
Esta información es producida y suministrada por el Instituto Nacional del Cáncer (NCI, por sus siglas en inglés). La información en este tema puede haber cambiado desde que se escribió. Para la información más actual, comuníquese con el Instituto Nacional del Cáncer a través del Internet en la página web http://cancer.gov o llame al 1-800-4-CANCER.
Introducción
El síndrome de Birt-Hogg-Dubé (BHD, o enfermedad de Birt-Hogg-Dubé) es un trastorno hamartomatoso de herencia autosómica dominante causado por variantes patogénicas germinales del gen FLCN.[
La gravedad de la enfermedad varía mucho. Las lesiones cutáneas por lo general aparecen durante la 3.ª o 4.ª décadas de vida, y aumentan de tamaño y número con la edad. Los quistes pulmonares suelen ser bilaterales y multifocales. La mayoría de las personas con quistes pulmonares son asintomáticas, pero tienen un riesgo alto de presentar neumotórax espontáneo.
Del 15 % al 30 % de las personas con síndrome de BHD presentarán tumores renales, a menudo bilaterales, multifocales y de crecimiento lento.[
Evolución natural
Las características clínicas del síndrome de BHD incluyen fibrofoliculomas o tricodiscomas (tipos de hamartomas cutáneos), quistes pulmonares o antecedentes de neumotórax y tumores renales de varios tipos histológicos. El síndrome de BHD se caracteriza por heterogeneidad fenotípica, y gran variabilidad en la gravedad de la enfermedad entre diferentes miembros de la misma familia y entre diferentes familias. Hasta la fecha, no hay evidencia de aumento del riesgo de cáncer de piel o de transformación maligna de estas lesiones hamartomatosas.
En 2001, en un estudio familiar se observó que los pacientes con diagnóstico clínico de síndrome de BHD eran 7 veces más propensos a presentar tumores renales que los familiares no afectados.[
Referencias:
- Toro JR, Wei MH, Glenn GM, et al.: BHD mutations, clinical and molecular genetic investigations of Birt-Hogg-Dubé syndrome: a new series of 50 families and a review of published reports. J Med Genet 45 (6): 321-31, 2008.
- Nickerson ML, Warren MB, Toro JR, et al.: Mutations in a novel gene lead to kidney tumors, lung wall defects, and benign tumors of the hair follicle in patients with the Birt-Hogg-Dubé syndrome. Cancer Cell 2 (2): 157-64, 2002.
- Birt AR, Hogg GR, Dubé WJ: Hereditary multiple fibrofolliculomas with trichodiscomas and acrochordons. Arch Dermatol 113 (12): 1674-7, 1977.
- Schmidt LS, Linehan WM: Molecular genetics and clinical features of Birt-Hogg-Dubé syndrome. Nat Rev Urol 12 (10): 558-69, 2015.
- Boza JC, Trindade EN, Peruzzo J, et al.: Skin manifestations of obesity: a comparative study. J Eur Acad Dermatol Venereol 26 (10): 1220-3, 2012.
- Sanfilippo AM, Barrio V, Kulp-Shorten C, et al.: Common pediatric and adolescent skin conditions. J Pediatr Adolesc Gynecol 16 (5): 269-83, 2003.
- Yosipovitch G, DeVore A, Dawn A: Obesity and the skin: skin physiology and skin manifestations of obesity. J Am Acad Dermatol 56 (6): 901-16; quiz 917-20, 2007.
- Pavlovich CP, Walther MM, Eyler RA, et al.: Renal tumors in the Birt-Hogg-Dubé syndrome. Am J Surg Pathol 26 (12): 1542-52, 2002.
- Benusiglio PR, Giraud S, Deveaux S, et al.: Renal cell tumour characteristics in patients with the Birt-Hogg-Dubé cancer susceptibility syndrome: a retrospective, multicentre study. Orphanet J Rare Dis 9: 163, 2014.
- Shuch B, Vourganti S, Ricketts CJ, et al.: Defining early-onset kidney cancer: implications for germline and somatic mutation testing and clinical management. J Clin Oncol 32 (5): 431-7, 2014.
- Graham RB, Nolasco M, Peterlin B, et al.: Nonsense mutations in folliculin presenting as isolated familial spontaneous pneumothorax in adults. Am J Respir Crit Care Med 172 (1): 39-44, 2005.
- Painter JN, Tapanainen H, Somer M, et al.: A 4-bp deletion in the Birt-Hogg-Dubé gene (FLCN) causes dominantly inherited spontaneous pneumothorax. Am J Hum Genet 76 (3): 522-7, 2005.
- Zbar B, Alvord WG, Glenn G, et al.: Risk of renal and colonic neoplasms and spontaneous pneumothorax in the Birt-Hogg-Dubé syndrome. Cancer Epidemiol Biomarkers Prev 11 (4): 393-400, 2002.
- Stamatakis L, Metwalli AR, Middelton LA, et al.: Diagnosis and management of BHD-associated kidney cancer. Fam Cancer 12 (3): 397-402, 2013.
Características genéticas
GenFLCN
El gen FLCN, es un gen supresor de tumores descubierto recientemente formado por 14 exones que se ubica en el cromosoma 17p11.2.[
Prevalencia
Se han descrito menos de 1000 familias afectadas por el síndrome de BHD en el mundo.[
Correlaciones entre genotipo y fenotipo
No se ha establecido una correlación entre variantes específicas del gen FLCN y las manifestaciones renales, pulmonares y cutáneas asociadas con el BHD. Sin embargo, las personas con una deleción en el tramo de policitosina del exón 11 quizás exhiban un riesgo más bajo de presentar cánceres renales relacionados al BHD que las personas con otras variantes de FLCN [
Referencias:
- Nickerson ML, Warren MB, Toro JR, et al.: Mutations in a novel gene lead to kidney tumors, lung wall defects, and benign tumors of the hair follicle in patients with the Birt-Hogg-Dubé syndrome. Cancer Cell 2 (2): 157-64, 2002.
- Schmidt LS, Nickerson ML, Warren MB, et al.: Germline BHD-mutation spectrum and phenotype analysis of a large cohort of families with Birt-Hogg-Dubé syndrome. Am J Hum Genet 76 (6): 1023-33, 2005.
- Toro JR, Wei MH, Glenn GM, et al.: BHD mutations, clinical and molecular genetic investigations of Birt-Hogg-Dubé syndrome: a new series of 50 families and a review of published reports. J Med Genet 45 (6): 321-31, 2008.
- Maffé A, Toschi B, Circo G, et al.: Constitutional FLCN mutations in patients with suspected Birt-Hogg-Dubé syndrome ascertained for non-cutaneous manifestations. Clin Genet 79 (4): 345-54, 2011.
- Kunogi M, Kurihara M, Ikegami TS, et al.: Clinical and genetic spectrum of Birt-Hogg-Dube syndrome patients in whom pneumothorax and/or multiple lung cysts are the presenting feature. J Med Genet 47 (4): 281-7, 2010.
- Rossing M, Albrechtsen A, Skytte AB, et al.: Genetic screening of the FLCN gene identify six novel variants and a Danish founder mutation. J Hum Genet 62 (2): 151-157, 2017.
- Savatt JM, Shimelis H, Moreno-De-Luca A, et al.: Frequency of truncating FLCN variants and Birt-Hogg-Dubé-associated phenotypes in a health care system population. Genet Med 24 (9): 1857-1866, 2022.
- Muller ME, Daccord C, Taffé P, et al.: Prevalence of Birt-Hogg-Dubé Syndrome Determined Through Epidemiological Data on Spontaneous Pneumothorax and Bayes Theorem. Front Med (Lausanne) 8: 631168, 2021.
Aspectos de la biología molecular
La identificación de un segundo golpe o mutación somática en la mayoría de los tumores renales asociados al síndrome de Birt-Hogg-Dubé (BHD) indica con firmeza que el FLCN es un gen supresor de tumores. Se han identificado mutaciones puntuales (variantes) somáticas en el alelo natural de FLCN, además de pérdida de heterocigosidad en el cromosoma 17p, aunque las mutaciones puntuales son el mecanismo más común de inactivación del segundo alelo del gen FLCN.[
Todavía no se han aclarado los mecanismos precisos por los que la inactivación del FLCN conduce a la carcinogénesis. Sin embargo, la foliculina, el producto proteínico del gen FLCN, es un componente del sistema sensor de energía celular. La foliculina, en combinación con 1 o 2 proteínas de interacción con foliculina, FNIP1 y FNIP2, interactúa con AMPK.[
Varios grupos han estudiado los efectos de la pérdida de la foliculina en la actividad de mTOR. Se demostró activación tisular específica de mTORC1 en un modelo de ratón con gen FLCN inactivado específico de riñón.[
Referencias:
- Vocke CD, Yang Y, Pavlovich CP, et al.: High frequency of somatic frameshift BHD gene mutations in Birt-Hogg-Dubé-associated renal tumors. J Natl Cancer Inst 97 (12): 931-5, 2005.
- Baba M, Hong SB, Sharma N, et al.: Folliculin encoded by the BHD gene interacts with a binding protein, FNIP1, and AMPK, and is involved in AMPK and mTOR signaling. Proc Natl Acad Sci U S A 103 (42): 15552-7, 2006.
- Hasumi H, Baba M, Hong SB, et al.: Identification and characterization of a novel folliculin-interacting protein FNIP2. Gene 415 (1-2): 60-7, 2008.
- Shaw RJ: LKB1 and AMP-activated protein kinase control of mTOR signalling and growth. Acta Physiol (Oxf) 196 (1): 65-80, 2009.
- Nahorski MS, Reiman A, Lim DH, et al.: Birt Hogg-Dubé syndrome-associated FLCN mutations disrupt protein stability. Hum Mutat 32 (8): 921-9, 2011.
- Baba M, Furihata M, Hong SB, et al.: Kidney-targeted Birt-Hogg-Dube gene inactivation in a mouse model: Erk1/2 and Akt-mTOR activation, cell hyperproliferation, and polycystic kidneys. J Natl Cancer Inst 100 (2): 140-54, 2008.
- Hasumi Y, Baba M, Ajima R, et al.: Homozygous loss of BHD causes early embryonic lethality and kidney tumor development with activation of mTORC1 and mTORC2. Proc Natl Acad Sci U S A 106 (44): 18722-7, 2009.
- Yan M, Gingras MC, Dunlop EA, et al.: The tumor suppressor folliculin regulates AMPK-dependent metabolic transformation. J Clin Invest 124 (6): 2640-50, 2014.
Manifestaciones clínicas
Las 3 características principales del síndrome de Birt-Hogg-Dubé (BHD) son los fibrofoliculomas o tricodiscomas, los quistes pulmonares y el neumotórax espontáneo, y los tumores renales.[
Lesiones cutáneas
Las personas con síndrome de BHD suelen presentar múltiples pápulas pequeñas en forma de cúpula, del mismo color de la piel, en la cara, el cuello y la parte superior del tronco. Estas manifestaciones dermatológicas características se llaman fibrofoliculomas o tricodiscomas (hamartoma del folículo piloso).[
Desde el punto de vista histológico, los fibrofoliculomas o tricodiscomas se caracterizan por múltiples hebras epiteliales anastomosantes que emanan de un folículo central. A veces el estroma está formado por tejido conjuntivo denso o rico en mucina y encapsula el componente epitelial.[
Quistes pulmonares y neumotórax espontáneo
En tomografía computarizada (TC) se observa que hay quistes pulmonares en el 85 % al 87 % de los pacientes con síndrome de BHD.[
En un estudio de 198 pacientes con BHD, los casos de neumotórax espontáneo fueron comparables entre hombres (20 %) y mujeres (29 %). Los primero neumotórax se presentaron entre los 22 y los 75 años.[
El cuadro clínico del neumotórax espontáneo varía desde ausencia de síntomas hasta disnea y dolor torácico. Los hallazgos clínicos incluyen taquipnea o murmullo respiratorio disminuido o ausente. Es posible que la investigación radiográfica exija el uso de una TC torácica de alta resolución para confirmar el diagnóstico porque la radiografía del tórax quizás no sea lo suficientemente sensible como para detectar un neumotórax loculado. Hasta el 75 % de los pacientes con antecedentes de neumotórax espontáneo presentarán un segundo caso de neumotórax espontáneo. Las diferencias en la notificación de la recidiva del neumotórax espontáneo quizás sean un reflejo de la eficacia de las diferentes modalidades de tratamiento.
Los hallazgos histológicos de las lesiones pleuropulmonares relacionadas con el síndrome de BHD incluyen bullas y quistes pleurales y subpleurales de pared delgada, quistes de aire intraparenquimatosos, vesículas pleurales y cambios compatibles con neumotórax espontáneo, además de cambios enfisematosos subyacentes en el parénquima pulmonar adyacente a las bullas.[
Tumores renales
Del 25 % al 35 % de las personas afectadas por el síndrome de BHD presentarán tumores renales,[
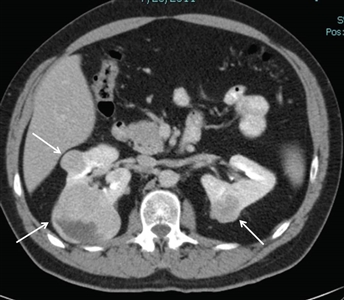
Los tumores más comunes son un híbrido de los tipos histológicos celulares oncocitoma y cromófobo, los llamados tumores híbridos oncocíticos, el carcinoma de células renales cromófobo y el oncocitoma renal. Solo el oncocitoma renal se considera un tumor benigno.[
Entre 70 pacientes con síndrome de BHD, tumores renales y una variante patogénica de FLCN analizados por los Institutos Nacionales de la Salud e identificados mediante revisión de la literatura, se notificó que 5 (7 %) fallecieron debido a RCC metastásico.[
Otras manifestaciones
Se notificaron oncocitomas de parótida multifocales bilaterales [
Cabe señalar que también se encontraron variantes germinales de FLCN en pacientes sin hallazgos cutáneos, pero con sospecha de síndrome de BHD debido a manifestaciones renales y pulmonares específicas.[
Además, se han notificado lipomas, angiolipomas,[
Aunque las observaciones epidemiológicas iniciales permitieron establecer un vínculo entre el síndrome de BHD y un aumento del riesgo de pólipos en el colon, en estudios epidemiológicos posteriores no se confirmó esta asociación.[
Referencias:
- Toro JR, Wei MH, Glenn GM, et al.: BHD mutations, clinical and molecular genetic investigations of Birt-Hogg-Dubé syndrome: a new series of 50 families and a review of published reports. J Med Genet 45 (6): 321-31, 2008.
- Schmidt LS, Nickerson ML, Warren MB, et al.: Germline BHD-mutation spectrum and phenotype analysis of a large cohort of families with Birt-Hogg-Dubé syndrome. Am J Hum Genet 76 (6): 1023-33, 2005.
- Schmidt LS, Linehan WM: Molecular genetics and clinical features of Birt-Hogg-Dubé syndrome. Nat Rev Urol 12 (10): 558-69, 2015.
- Toro JR, Glenn G, Duray P, et al.: Birt-Hogg-Dubé syndrome: a novel marker of kidney neoplasia. Arch Dermatol 135 (10): 1195-202, 1999.
- Graham RB, Nolasco M, Peterlin B, et al.: Nonsense mutations in folliculin presenting as isolated familial spontaneous pneumothorax in adults. Am J Respir Crit Care Med 172 (1): 39-44, 2005.
- Painter JN, Tapanainen H, Somer M, et al.: A 4-bp deletion in the Birt-Hogg-Dubé gene (FLCN) causes dominantly inherited spontaneous pneumothorax. Am J Hum Genet 76 (3): 522-7, 2005.
- Vernooij M, Claessens T, Luijten M, et al.: Birt-Hogg-Dubé syndrome and the skin. Fam Cancer 12 (3): 381-5, 2013.
- Toro JR, Pautler SE, Stewart L, et al.: Lung cysts, spontaneous pneumothorax, and genetic associations in 89 families with Birt-Hogg-Dubé syndrome. Am J Respir Crit Care Med 175 (10): 1044-53, 2007.
- Matsumoto K, Lim D, Pharoah PD, et al.: A systematic review assessing the existence of pneumothorax-only variants of FLCN. Implications for lifelong surveillance of renal tumours. Eur J Hum Genet 29 (11): 1595-1600, 2021.
- Zbar B, Alvord WG, Glenn G, et al.: Risk of renal and colonic neoplasms and spontaneous pneumothorax in the Birt-Hogg-Dubé syndrome. Cancer Epidemiol Biomarkers Prev 11 (4): 393-400, 2002.
- Pavlovich CP, Walther MM, Eyler RA, et al.: Renal tumors in the Birt-Hogg-Dubé syndrome. Am J Surg Pathol 26 (12): 1542-52, 2002.
- Pavlovich CP, Grubb RL, Hurley K, et al.: Evaluation and management of renal tumors in the Birt-Hogg-Dubé syndrome. J Urol 173 (5): 1482-6, 2005.
- Shuch B, Vourganti S, Ricketts CJ, et al.: Defining early-onset kidney cancer: implications for germline and somatic mutation testing and clinical management. J Clin Oncol 32 (5): 431-7, 2014.
- Sattler EC, Reithmair M, Steinlein OK: Kidney cancer characteristics and genotype-phenotype-correlations in Birt-Hogg-Dubé syndrome. PLoS One 13 (12): e0209504, 2018.
- Howlader N, Noone AM, Krapcho M, et al.: SEER Cancer Statistics Review (CSR) 1975-2017. Bethesda, Md: National Cancer Institute, 2020.
Available online . Last accessed February 7, 2025. - Vocke CD, Yang Y, Pavlovich CP, et al.: High frequency of somatic frameshift BHD gene mutations in Birt-Hogg-Dubé-associated renal tumors. J Natl Cancer Inst 97 (12): 931-5, 2005.
- da Silva NF, Gentle D, Hesson LB, et al.: Analysis of the Birt-Hogg-Dubé (BHD) tumour suppressor gene in sporadic renal cell carcinoma and colorectal cancer. J Med Genet 40 (11): 820-4, 2003.
- Khoo SK, Kahnoski K, Sugimura J, et al.: Inactivation of BHD in sporadic renal tumors. Cancer Res 63 (15): 4583-7, 2003.
- Liu V, Kwan T, Page EH: Parotid oncocytoma in the Birt-Hogg-Dubé syndrome. J Am Acad Dermatol 43 (6): 1120-2, 2000.
- Vinit J, Friedel J, Bielefeld P, et al.: [Birt-Hogg-Dubé syndrome and multiple recurrent tumors]. Rev Med Interne 32 (3): e40-2, 2011.
- Maffé A, Toschi B, Circo G, et al.: Constitutional FLCN mutations in patients with suspected Birt-Hogg-Dubé syndrome ascertained for non-cutaneous manifestations. Clin Genet 79 (4): 345-54, 2011.
- Chung JY, Ramos-Caro FA, Beers B, et al.: Multiple lipomas, angiolipomas, and parathyroid adenomas in a patient with Birt-Hogg-Dube syndrome. Int J Dermatol 35 (5): 365-7, 1996.
- Vincent A, Farley M, Chan E, et al.: Birt-Hogg-Dubé syndrome: two patients with neural tissue tumors. J Am Acad Dermatol 49 (4): 717-9, 2003.
- Drummond C, Grigoris I, Dutta B: Birt-Hogg-Dubé syndrome and multinodular goitre. Australas J Dermatol 43 (4): 301-4, 2002.
- Welsch MJ, Krunic A, Medenica MM: Birt-Hogg-Dubé Syndrome. Int J Dermatol 44 (8): 668-73, 2005.
- Tomassetti S, Carloni A, Chilosi M, et al.: Pulmonary features of Birt-Hogg-Dubé syndrome: cystic lesions and pulmonary histiocytoma. Respir Med 105 (5): 768-74, 2011.
- Walter P, Kirchhof B, Korge B, et al.: Flecked chorioretinopathy associated with Birt-Hogg-Dubé syndrome. Graefes Arch Clin Exp Ophthalmol 235 (6): 359-61, 1997.
- Nahorski MS, Lim DH, Martin L, et al.: Investigation of the Birt-Hogg-Dube tumour suppressor gene (FLCN) in familial and sporadic colorectal cancer. J Med Genet 47 (6): 385-90, 2010.
- van de Beek I, Glykofridis IE, Wolthuis RMF, et al.: No evidence for increased prevalence of colorectal carcinoma in 399 Dutch patients with Birt-Hogg-Dubé syndrome. Br J Cancer 122 (4): 590-594, 2020.
Atención médica
Evaluación del riesgo del síndrome de Birt-Hogg-Dubé
Pruebas genéticas
El FLCN es el único gen del que se conoce su asociación con el síndrome de Birt-Hogg-Dubé (BHD). Está ubicado en el cromosoma 17p11.2.[
Se indica el uso de pruebas genéticas a cargo de laboratorios con certificación según las Enmiendas para el Mejoramiento de Laboratorios Clínicos (CLIA) para todas las personas con un presunto síndrome de BHD o en quienes ya se confirmó la afectación, entre ellos quienes presenten las siguientes características:
- 5 o más pápulas en la cara o el tronco, y por lo menos 1 fibrofoliculoma confirmado mediante análisis histológico,[
5 ] con historia familiar compatible con síndrome de BHD o sin estos antecedentes familiares. - Historia familiar compatible con el síndrome de BHD y un fibrofoliculoma único, un tumor renal único o antecedentes personales de neumotórax espontáneo.
- Tumores cromófobos múltiples y bilaterales, o tumores renales híbridos oncocíticos.
- 1 solo tumor cromófobo o 1 tumor híbrido oncocítico acompañado de una historia familiar compatible con cáncer renal de cualquiera de los tipos de células renales mencionados antes.
- Una historia familiar de neumotórax espontáneo primario de herencia autosómica dominante sin antecedentes de quistes pulmonares.
Asesoramiento genético
El síndrome de BHD se hereda de manera autosómica dominante. Si un progenitor de un probando está afectado clínicamente o tiene una variante patogénica de FLCN , los hermanos o hermanas del probando tienen una probabilidad del 50 % de heredar la variante. La gravedad clínica no es predecible. El diagnóstico prenatal de BHD es posible durante el embarazo con un 50 % de probabilidad de heredar una variante patogénica de FLCN si la variante que causa la enfermedad se ha identificado en un miembro de la familia afectado.
En el resumen Evaluación del riesgo de cáncer y asesoramiento genético se proporciona más información acerca de estos temas:
- Para obtener más información sobre el diagnóstico prenatal de los síndromes de cáncer hereditario, consultar la sección
Pruebas genéticas y técnicas de reproducción asistida . - Para obtener más información sobre la herencia autosómica dominante, consultar la sección
Análisis de la historia familiar . - Para obtener más información sobre las pruebas genéticas para detectar variantes patogénicas en miembros de una familia, consultar la sección
Pruebas genéticas en cascada en los miembros de una familia .
Diagnóstico clínico
Las 3 características principales del síndrome de BHD son las lesiones cutáneas, las manifestaciones pulmonares (quistes en el pulmón y neumotórax espontáneo) y los tumores renales.[
El diagnóstico dermatológico del síndrome de BHD se establece en personas que tienen 5 o más pápulas en la cara o el tronco, y por lo menos 1 fibrofoliculoma confirmado por análisis histológico.[
- Criterios principales
- Por lo menos 5 fibrofoliculomas o tricodiscomas (al menos 1 confirmado por análisis histológico), y de inicio en la edad adulta.
- Variante patogénica germinal de FLCN.
- Criterios secundarios
- Quistes pulmonares múltiples: quistes pulmonares bilaterales y basales sin otra causa aparente, con neumotórax primario espontáneo o sin este.
- Cáncer renal: cáncer renal multifocal, bilateral o de inicio temprano (edad <50 años), o cáncer renal de tipo histológico mixto cromófobo y oncocítico.
- Un familiar de primer grado con síndrome de BHD.
Diagnóstico diferencial
Es importante distinguir entre el carcinoma de células renales propio del síndrome de BHD y el carcinoma de células renales esporádico porque esto quizás repercuta en el tratamiento. El uso de pruebas genéticas para detectar una variante patogénica en FLCN, una historia familiar de BHD, o la presencia de manifestaciones extrarrenales del BHD son útiles para establecer el diagnóstico de esta afección. Debido a que se pueden observar variantes histológicas del cáncer de riñón asociadas al síndrome de BHD, a menudo es necesario determinar el diagnóstico histológico para ayudar a diferenciar entre tumores benignos (oncocitomas) y los que tienen potencial maligno (carcinoma de células renales cromófobo, de células claras y papilar).[
El diagnóstico diferencial de los quistes pulmonares incluye la linfangioleiomiomatosis (LAM); distinguir la LAM del síndrome de BHD es un reto clínico. En un estudio se propuso un conjunto de hallazgos que permiten diferenciar el síndrome de BHD y la LAM.[
Vigilancia
Los pacientes con síndrome de BHD exhiben 2 cuadros clínicos iniciales principales. Con mayor frecuencia, las personas presentan una historia familiar documentada de síndrome de BHD. Otro cuadro clínico inicial ocurre en personas sin una historia familiar compatible con el síndrome de BHD o que desconocen su historia familiar. En el primer escenario clínico, si el paciente tiene un familiar biológico en el que se estableció un diagnóstico genético y en quien se identificó una variante patogénica de FLCN, es posible que el paciente decida comenzar la evaluación con el asesoramiento genético y las pruebas de la variante patogénica.
La vigilancia clínica para las personas en riesgo de BHD incluye exámenes dermatológicos, radiológicos e histológicos para identificar lesiones cutáneas características, tumores renales y quistes pulmonares, con o sin antecedentes de neumotórax espontáneo. No todas las personas en riesgo exhiben todas las características, y es posible que algunos familiares no presenten hallazgos fenotípicos discernibles (es decir, son portadores de variantes de FLCNdeletéreas no afectados desde el punto de vista clínico). Este escenario clínico es cada vez más frecuente a medida que aumenta el número de genes relacionados con el síndrome para los que se pueden ofrecer pruebas de variantes patogénicas en el ámbito clínico. En la mayoría de los trastornos, todavía no se ha caracterizado bien la evolución natural en las personas con anomalías genéticas que son normales desde el punto de vista clínico. Estas características principales del BHD se describen en la sección
Las decisiones sobre la vigilancia de por vida para los síndromes hereditarios de carcinoma de células renales deben tener en cuenta tanto los riesgos como los beneficios. Del 15 % al 29 % de las personas afectadas por el síndrome de BHD presentarán tumores renales,[
La tomografía computarizada (TC) contrastada o las imágenes por resonancia magnética (IRM) son modalidades útiles para la detección de los tumores renales asociados con el síndrome de BHD.[
Nivel de evidencia: 5
Tratamiento
Cutáneo
Se ha usado crioterapia, electrodesecación, cirugía y terapia láser con buenos resultados cosméticos, pero a menudo hay recaída porque las lesiones son una manifestación de una afección cutánea hereditaria.[
Nivel de evidencia: 5
Renal
La nefrectomía parcial es el tratamiento de elección para el abordaje de las neoplasias de riñón relacionadas con el síndrome de BHD, con el fin de conservar el funcionamiento renal óptimo a largo plazo en pacientes con riesgo de múltiples tumores renales primarios. Sin embargo, la cirugía con conservación renal depende del tamaño y la ubicación de los tumores que se encuentran durante la cirugía. Cuando se planifica el tratamiento quirúrgico, es importante incorporar el conocimiento del riesgo acumulado alto de tumores renales multifocales y bilaterales en este síndrome. En general, los tumores renales de menos de 3 cm de diámetro los puede vigilar de cerca el cirujano especialista en urología oncológica y es posible que no se requiera una cirugía inmediata.[
La vigilancia de personas y familiares en riesgo incluye IRM o TC abdominales o pélvicas, además de la evaluación de tumores renales a cargo de urólogos cirujanos y radiólogos con experiencia en el tratamiento de estos pacientes complicados. El uso de una prueba genética para la identificación temprana de los familiares en riesgo mejora la certeza diagnóstica y elimina los costosos y estresantes procedimientos de detección en los familiares en riesgo que no heredaron la variante causal de enfermedad presente en la familia.
Nivel de evidencia: 4
Neumotórax espontáneo
El tratamiento del neumotórax espontáneo en pacientes con el síndrome de BHD es similar al de la población general.[
El cuadro clínico inicial del neumotórax espontáneo en pacientes con síndrome de BHD es variable. El tratamiento se determina a partir de la afección pulmonar subyacente y el estado general de salud del paciente. En un estudio se notificó que de 101 pacientes con neumotórax espontáneo, 78 necesitaron una intervención médica, y 23 se abordaron solo con observación.[
Nivel de evidencia: 4
Referencias:
- Schmidt LS, Warren MB, Nickerson ML, et al.: Birt-Hogg-Dubé syndrome, a genodermatosis associated with spontaneous pneumothorax and kidney neoplasia, maps to chromosome 17p11.2. Am J Hum Genet 69 (4): 876-82, 2001.
- Schmidt LS, Nickerson ML, Warren MB, et al.: Germline BHD-mutation spectrum and phenotype analysis of a large cohort of families with Birt-Hogg-Dubé syndrome. Am J Hum Genet 76 (6): 1023-33, 2005.
- Toro JR, Wei MH, Glenn GM, et al.: BHD mutations, clinical and molecular genetic investigations of Birt-Hogg-Dubé syndrome: a new series of 50 families and a review of published reports. J Med Genet 45 (6): 321-31, 2008.
- Benhammou JN, Vocke CD, Santani A, et al.: Identification of intragenic deletions and duplication in the FLCN gene in Birt-Hogg-Dubé syndrome. Genes Chromosomes Cancer 50 (6): 466-77, 2011.
- Toro JR, Glenn G, Duray P, et al.: Birt-Hogg-Dubé syndrome: a novel marker of kidney neoplasia. Arch Dermatol 135 (10): 1195-202, 1999.
- Menko FH, van Steensel MA, Giraud S, et al.: Birt-Hogg-Dubé syndrome: diagnosis and management. Lancet Oncol 10 (12): 1199-206, 2009.
- Pavlovich CP, Grubb RL, Hurley K, et al.: Evaluation and management of renal tumors in the Birt-Hogg-Dubé syndrome. J Urol 173 (5): 1482-6, 2005.
- Gupta N, Seyama K, McCormack FX: Pulmonary manifestations of Birt-Hogg-Dubé syndrome. Fam Cancer 12 (3): 387-96, 2013.
- Zbar B, Alvord WG, Glenn G, et al.: Risk of renal and colonic neoplasms and spontaneous pneumothorax in the Birt-Hogg-Dubé syndrome. Cancer Epidemiol Biomarkers Prev 11 (4): 393-400, 2002.
- Stamatakis L, Metwalli AR, Middelton LA, et al.: Diagnosis and management of BHD-associated kidney cancer. Fam Cancer 12 (3): 397-402, 2013.
- Johannesma PC, van de Beek I, van der Wel TJWT, et al.: Renal imaging in 199 Dutch patients with Birt-Hogg-Dubé syndrome: Screening compliance and outcome. PLoS One 14 (3): e0212952, 2019.
- Jacob CI, Dover JS: Birt-Hogg-Dube syndrome: treatment of cutaneous manifestations with laser skin resurfacing. Arch Dermatol 137 (1): 98-9, 2001.
- Gambichler T, Wolter M, Altmeyer P, et al.: Treatment of Birt-Hogg-Dubé syndrome with erbium:YAG laser. J Am Acad Dermatol 43 (5 Pt 1): 856-8, 2000.
- Kahle B, Hellwig S, Schulz T: [Multiple mantleomas in Birt-Hogg-Dubé syndrome: successful therapy with CO2 laser] Hautarzt 52 (1): 43-6, 2001.
- Toro JR, Pautler SE, Stewart L, et al.: Lung cysts, spontaneous pneumothorax, and genetic associations in 89 families with Birt-Hogg-Dubé syndrome. Am J Respir Crit Care Med 175 (10): 1044-53, 2007.
Pronóstico
La causa principal de morbilidad y mortalidad en el síndrome de Birt-Hogg-Dubé (BHD) está relacionada con las lesiones renales. Debido a la rareza del síndrome de BHD, es difícil generar datos sólidos de supervivencia general en poblaciones de pacientes con este síndrome; sin embargo, cuando los pacientes se tratan con una estrategia apropiada de vigilancia e intervención, su esperanza de vida no debe ser significativamente diferente a la de las personas de la población general emparejadas.
Si bien la mayoría de los pacientes obtienen excelentes resultados cuando los tumores se detectan temprano y se extirpan mediante cirugía, hay riesgo de metástasis con tumores más grandes y el tratamiento óptimo de la enfermedad metastásica no está claro.[
Referencias:
- Johannesma PC, van de Beek I, van der Wel TJWT, et al.: Renal imaging in 199 Dutch patients with Birt-Hogg-Dubé syndrome: Screening compliance and outcome. PLoS One 14 (3): e0212952, 2019.
Indicaciones futuras
Desde que en 2001 se identificó el gen FLCN, responsable del síndrome de Birt-Hogg-Dubé, en varios estudios se ha aclarado su función y las posibles correlaciones entre genotipo y fenotipo. Aunque la vigilancia seguida de resección quirúrgica sigue siendo el pilar del abordaje de la enfermedad, las mejoras en la detección temprana y en las intervenciones moleculares tempranas quizás modifiquen la evolución de esta enfermedad en el riñón al disminuir la incidencia de las manifestaciones renales evidentes o letales. Una mejor comprensión del funcionamiento bioquímico de la proteína FLCN debe proporcionar información sobre la identificación y validación del tratamiento médico para la enfermedad localizada, localmente avanzada y metastásica.
Actualizaciones más recientes a este resumen (02 / 18 / 2025)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes introducidos en este resumen a partir de la fecha arriba indicada.
Se incorporaron cambios editoriales en este resumen.
El
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre la genética del síndrome de Birt-Hogg-Dubé. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Síndrome de Birt-Hogg-Dubé son:
- Alexandra Perez Lebensohn, MS, CGC (National Cancer Institute)
- Brian Matthew Shuch, MD (UCLA Health)
- Ramaprasad Srinivasan, MD, PhD (National Cancer Institute)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como "En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]".
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre la genética del cáncer. PDQ Síndrome de Birt-Hogg-Dubé. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en:
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar
Cláusula sobre el descargo de responsabilidad
La información en estos resúmenes no se debe utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del
Última revisión: 2025-02-18
Esta información no reemplaza el consejo de un médico. Ignite Healthwise, LLC, niega toda garantía y responsabilidad por el uso de esta información. El uso que usted haga de esta información implica que usted acepta los
Healthwise, Healthwise para cada decisión de la salud, y el logo de Healthwise son marcas de fábrica de Ignite Healthwise, LLC.
Page Footer
Quiero...
Audiencia
Sitios seguros para miembros
Información sobre The Cigna Group
Aviso legal
Los planes individuales y familiares de seguro médico y dental están asegurados por Cigna Health and Life Insurance Company (CHLIC), Cigna HealthCare of Arizona, Inc., Cigna HealthCare of Illinois, Inc., Cigna HealthCare of Georgia, Inc., Cigna HealthCare of North Carolina, Inc., Cigna HealthCare of South Carolina, Inc. y Cigna HealthCare of Texas, Inc. Los planes de beneficios de salud y de seguro de salud de grupo están asegurados o administrados por CHLIC, Connecticut General Life Insurance Company (CGLIC) o sus afiliadas (puedes ver
Todas las pólizas de seguros y los planes de beneficios de grupo contienen exclusiones y limitaciones. Para conocer la disponibilidad, los costos y detalles completos de la cobertura, comunícate con un agente autorizado o con un representante de ventas de Cigna. Este sitio web no está dirigido a los residentes de New Mexico.