Comprar planes
Comprar tu propia cobertura
Planes a través de tu empleador
Conoce sobre los beneficios médicos, dentales, de farmacia y voluntarios que tu empleador puede ofrecer.
Aprender
¿Vives o trabajas fuera del país?
Tratamiento del melanoma infantil (PDQ®) : Tratamiento - información para profesionales de salud [NCI]
Esta información es producida y suministrada por el Instituto Nacional del Cáncer (NCI, por sus siglas en inglés). La información en este tema puede haber cambiado desde que se escribió. Para la información más actual, comuníquese con el Instituto Nacional del Cáncer a través del Internet en la página web http://cancer.gov o llame al 1-800-4-CANCER.
Incidencia
El melanoma, aunque es un cáncer poco frecuente en los niños, es el cáncer de piel más común durante la niñez, seguido del carcinoma de células basales y el carcinoma de células escamosas.[
En los Estados Unidos, se diagnostican alrededor de 300 casos de melanoma cada año en pacientes menores de 20 años; cifra que representa el 0,3 % de todos los casos nuevos de melanoma.[
La incidencia anual de melanoma en los Estados Unidos aumenta con la edad, según se indica en la
En la
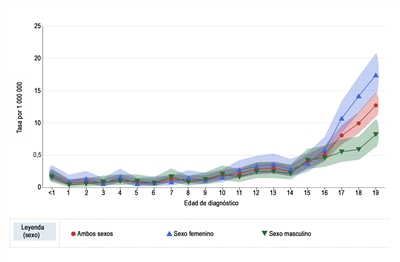
La incidencia de melanoma en pediatría (edad 0–19 años) aumentó en promedio un 1,6 % por año entre 1975 y 1996. Como se observa en la
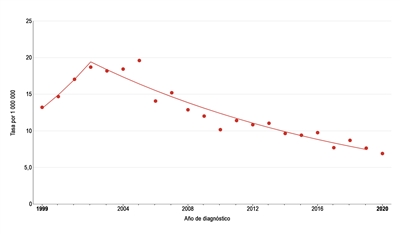
En un estudio retrospectivo de 22 524 informes patológicos de la piel de pacientes menores de 20 años, se identificaron 38 melanomas; entre ellos, 33 en adolescentes de 15 a 19 años. Los investigadores informaron que fue necesario extirpar 479,8 lesiones para identificar 1 melanoma; esto es 20 veces más que la cantidad necesaria en la población adulta.[
Referencias:
- Sasson M, Mallory SB: Malignant primary skin tumors in children. Curr Opin Pediatr 8 (4): 372-7, 1996.
- Fishman C, Mihm MC, Sober AJ: Diagnosis and management of nevi and cutaneous melanoma in infants and children. Clin Dermatol 20 (1): 44-50, 2002 Jan-Feb.
- Hamre MR, Chuba P, Bakhshi S, et al.: Cutaneous melanoma in childhood and adolescence. Pediatr Hematol Oncol 19 (5): 309-17, 2002 Jul-Aug.
- Ceballos PI, Ruiz-Maldonado R, Mihm MC: Melanoma in children. N Engl J Med 332 (10): 656-62, 1995.
- Schmid-Wendtner MH, Berking C, Baumert J, et al.: Cutaneous melanoma in childhood and adolescence: an analysis of 36 patients. J Am Acad Dermatol 46 (6): 874-9, 2002.
- Pappo AS: Melanoma in children and adolescents. Eur J Cancer 39 (18): 2651-61, 2003.
- Huynh PM, Grant-Kels JM, Grin CM: Childhood melanoma: update and treatment. Int J Dermatol 44 (9): 715-23, 2005.
- Christenson LJ, Borrowman TA, Vachon CM, et al.: Incidence of basal cell and squamous cell carcinomas in a population younger than 40 years. JAMA 294 (6): 681-90, 2005.
- National Cancer Institute: SEER Stat Fact Sheets: Melanoma of the Skin. Bethesda, Md: National Cancer Institute.
Available online . Last accessed December 15, 2023. - National Cancer Institute: NCCR*Explorer: An interactive website for NCCR cancer statistics. Bethesda, MD: National Cancer Institute.
Available online . Last accessed February 25, 2025. - Paulson KG, Gupta D, Kim TS, et al.: Age-Specific Incidence of Melanoma in the United States. JAMA Dermatol 156 (1): 57-64, 2020.
- Moscarella E, Zalaudek I, Cerroni L, et al.: Excised melanocytic lesions in children and adolescents - a 10-year survey. Br J Dermatol 167 (2): 368-73, 2012.
Factores de riesgo
Las afecciones relacionadas con un aumento del riesgo de melanoma en niños y adolescentes son las siguientes:
- Nevos melanocíticos gigantes.[
1 ] - Xeroderma pigmentoso. Este trastorno recesivo poco frecuente se caracteriza por una sensibilidad extrema a la luz solar, queratosis y diferentes manifestaciones neurológicas.[
1 ] Para obtener más información sobre el xeroderma pigmentoso, consultarGenética del cáncer de piel . - Inmunodeficiencia o inmunodepresión.[
2 ] - Retinoblastoma hereditario.[
3 ] - Síndrome de Werner.[
4 ,5 ] - Melanosis neurocutánea. Este trastorno inusual surge en el contexto de nevos melanocíticos congénitos y se caracteriza por nevos congénitos grandes o múltiples en la piel y melanosis meníngea o melanoma. Alrededor del 2,5 % de los pacientes con nevos congénitos grandes presentan esta afección; el riesgo es más alto en quienes tienen muchos nevos satelitales.[
6 ,7 ]Los pacientes con melanoma en el sistema nervioso central (SNC) y síndrome de nevos melanocíticos congénitos tienen un pronóstico desfavorable y una mortalidad del 100 %. La mayoría de estos pacientes tienen variantes de NRAS. Por lo tanto, los inhibidores de la vía de la proteína–cinasa activada por mitógenos podrían usarse para el tratamiento de esta enfermedad. Cuatro niños tratados con un inhibidor de MEK presentaron mejorías sintomáticas transitorias; sin embargo, todos los pacientes murieron debido a progresión de la enfermedad.[
8 ] En un registro alemán se identificaron 5 niños con melanomas en el SNC que presentaban melanocitosis neurocutánea.[9 ] Todos los pacientes murieron entre 0,3 y 0,8 años después del diagnóstico. - Antecedentes familiares de melanoma.
Los rasgos fenotípicos relacionados con un aumento del riesgo de melanoma en adultos y que también se han documentado en niños y adolescentes con melanoma son los siguientes:[
- Exposición a los rayos ultravioleta de la luz solar. Una mayor exposición a la radiación ultravioleta (UV) ambiental aumenta el riesgo de contraer la enfermedad.
- Cabello rojo.
- Ojos azules.
- Poca capacidad para broncearse.
- Pecas.
- Nevos displásicos.
- Número elevado de nevos melanocíticos.
Los genes que presentan variantes patogénicas germinales asociadas con aumento del riesgo de melanoma en niños son los siguientes:
- Gen MC1R. Un consorcio internacional realizó una revisión retrospectiva de las variantes patogénicas germinales del gen MC1R.[
17 ] Los investigadores analizaron los datos de 233 pacientes jóvenes (edad ≤20 años), 932 pacientes adultos (edad ≥35 años) y 932 adultos sanos que sirvieron como grupo de control. Las variantes de MC1R fueron más frecuentes en los niños y adolescentes con melanoma que en los adultos con melanoma. Este resultado fue más evidente en pacientes de 18 años o menos. - Gen CDKN2A (gen p16). El melanoma familiar explica del 8 % al 12 % de los casos de melanoma. Se han descrito variantes patogénicas germinales de p16 en hasta un 7 % de las familias con 2 familiares de primer grado afectados por melanoma, y en hasta un 80 % de las familias con 1 miembro afectado por múltiples melanomas primarios.[
18 ] En un estudio prospectivo de 60 familias con más de 3 miembros con melanoma,[19 ] se encontró que la mitad de estas familias tenía una variante patogénica germinal de CDKN2A. Con independencia del estado de CDKN2A, el porcentaje de pacientes con melanoma infantil en las familias con predisposición al melanoma es entre 6 y 28 veces el porcentaje de la población general de pacientes con melanoma en los Estados Unidos. En las familias que portan una variante de CDKN2A, los niños con melanoma exhibieron una propensión significativa a tener múltiples melanomas en comparación con los familiares que tenían más de 20 años en el momento del diagnóstico (71 vs. 38 %, respectivamente; P = 0,004). Las familias que portan una variante de CDKN2A tuvieron porcentajes significativamente más altos de pacientes pediátricos con melanoma en comparación con las familias que no portan una variante de CDKN2A (11,1 vs. 2,5 %, respectivamente; P = 0,004). - Variante de MITF p.E318K. En una serie de pacientes menores de 21 años, 3 de 123 pacientes (2,4 %) exhibían una sustitución en MITF que se consideró que confiere un riesgo moderado de melanoma cutáneo.[
20 ,21 ]
Referencias:
- Ceballos PI, Ruiz-Maldonado R, Mihm MC: Melanoma in children. N Engl J Med 332 (10): 656-62, 1995.
- Pappo AS: Melanoma in children and adolescents. Eur J Cancer 39 (18): 2651-61, 2003.
- Kleinerman RA, Tucker MA, Tarone RE, et al.: Risk of new cancers after radiotherapy in long-term survivors of retinoblastoma: an extended follow-up. J Clin Oncol 23 (10): 2272-9, 2005.
- Shibuya H, Kato A, Kai N, et al.: A case of Werner syndrome with three primary lesions of malignant melanoma. J Dermatol 32 (9): 737-44, 2005.
- Kleinerman RA, Yu CL, Little MP, et al.: Variation of second cancer risk by family history of retinoblastoma among long-term survivors. J Clin Oncol 30 (9): 950-7, 2012.
- Hale EK, Stein J, Ben-Porat L, et al.: Association of melanoma and neurocutaneous melanocytosis with large congenital melanocytic naevi--results from the NYU-LCMN registry. Br J Dermatol 152 (3): 512-7, 2005.
- Makkar HS, Frieden IJ: Neurocutaneous melanosis. Semin Cutan Med Surg 23 (2): 138-44, 2004.
- Kinsler VA, O'Hare P, Jacques T, et al.: MEK inhibition appears to improve symptom control in primary NRAS-driven CNS melanoma in children. Br J Cancer 116 (8): 990-993, 2017.
- Abele M, Forchhammer S, Eigentler TK, et al.: Melanoma of the central nervous system based on neurocutaneous melanocytosis in childhood: A rare but fatal condition. Pediatr Blood Cancer 71 (4): e30859, 2024.
- Heffernan AE, O'Sullivan A: Pediatric sun exposure. Nurse Pract 23 (7): 67-8, 71-8, 83-6, 1998.
- Berg P, Lindelöf B: Differences in malignant melanoma between children and adolescents. A 35-year epidemiological study. Arch Dermatol 133 (3): 295-7, 1997.
- Elwood JM, Jopson J: Melanoma and sun exposure: an overview of published studies. Int J Cancer 73 (2): 198-203, 1997.
- Strouse JJ, Fears TR, Tucker MA, et al.: Pediatric melanoma: risk factor and survival analysis of the surveillance, epidemiology and end results database. J Clin Oncol 23 (21): 4735-41, 2005.
- Whiteman DC, Valery P, McWhirter W, et al.: Risk factors for childhood melanoma in Queensland, Australia. Int J Cancer 70 (1): 26-31, 1997.
- Tucker MA, Fraser MC, Goldstein AM, et al.: A natural history of melanomas and dysplastic nevi: an atlas of lesions in melanoma-prone families. Cancer 94 (12): 3192-209, 2002.
- Ducharme EE, Silverberg NB: Pediatric malignant melanoma: an update on epidemiology, detection, and prevention. Cutis 84 (4): 192-8, 2009.
- Pellegrini C, Botta F, Massi D, et al.: MC1R variants in childhood and adolescent melanoma: a retrospective pooled analysis of a multicentre cohort. Lancet Child Adolesc Health 3 (5): 332-342, 2019.
- Soufir N, Avril MF, Chompret A, et al.: Prevalence of p16 and CDK4 germline mutations in 48 melanoma-prone families in France. The French Familial Melanoma Study Group. Hum Mol Genet 7 (2): 209-16, 1998.
- Goldstein AM, Stidd KC, Yang XR, et al.: Pediatric melanoma in melanoma-prone families. Cancer 124 (18): 3715-3723, 2018.
- Pellegrini C, Raimondi S, Di Nardo L, et al.: Melanoma in children and adolescents: analysis of susceptibility genes in 123 Italian patients. J Eur Acad Dermatol Venereol 36 (2): 213-221, 2022.
- Guhan SM, Artomov M, McCormick S, et al.: Cancer risks associated with the germline MITF(E318K) variant. Sci Rep 10 (1): 17051, 2020.
Evaluación diagnóstica
El diagnóstico de melanoma infantil a veces es difícil, muchas de estas lesiones se confunden con las llamadas lesiones melanocíticas con potencial maligno desconocido.[
La evaluación diagnóstica del melanoma infantil incluye los siguientes aspectos:
- Biopsia o extirpación. La biopsia o extirpación es necesaria para diagnosticar cualquier cáncer de piel y decidir si se necesita más tratamiento. Aunque los carcinomas de células basales y los carcinoma de células escamosas por lo general se curan con cirugía sola, el melanoma exige mayor consideración por su potencial de metástasis. El ancho de los márgenes quirúrgicos para la extirpación de un melanoma se determina según el sitio, el tamaño y el grosor de la lesión; y oscila entre 0,5 cm para las lesiones in situ y 2 cm o más para las lesiones más gruesas.[
4 ] En algunos casos específicos es posible que se necesite una extirpación amplia con injerto de piel con el fin de obtener márgenes sin compromiso tumoral. - Evaluación ganglionar. La valoración de los ganglios linfáticos regionales mediante biopsia de ganglio linfático centinela se ha vuelto un procedimiento de rutina en muchos centros.[
5 ,6 ] Se recomienda obtener la biopsia de ganglio linfático centinela en los pacientes con lesiones que miden 0,8 cm o más,[4 ] y en los pacientes con lesiones de menos de 0,8 cm que presentan ulceración u otras características desfavorables como invasión linfovascular, tasa mitótica alta, edad temprana o biopsia con márgenes positivos para compromiso tumoral.[4 ,5 ,7 ,8 ,9 ]Las indicaciones para este tipo de biopsia en pacientes con melanomas spitzoides no se han definido con claridad. En una revisión sistemática de 541 pacientes con tumores de Spitz atípicos, 303 (56 %) se sometieron a biopsia de ganglio centinela y 119 (39 %) tenían compromiso de un ganglio centinela. De estos pacientes, 97 se sometieron a otra disección ganglionar y se identificaron ganglios afectados en 18 de ellos (19 %).[
10 ] A pesar de la alta frecuencia de metástasis ganglionares, solo 6 pacientes presentaron enfermedad diseminada. Este resultado desafía el beneficio pronóstico y terapéutico del procedimiento en niños con este tipo de lesiones. En el futuro, los marcadores moleculares, como la presencia de variantes en el promotor de TERT quizás ayuden a identificar qué pacientes se podrían beneficiar de este procedimiento.[11 ]En la sección
Tratamiento del melanoma infantil se explica la función de la disección ganglionar completa después de identificar compromiso de un ganglio linfático centinela y la utilidad de las terapias adyuvantes en estos pacientes. - Evaluación de laboratorio y pruebas con imágenes. Los pacientes que presentan un melanoma convencional o de tipo adulto deben someterse a evaluación mediante pruebas de laboratorio e imágenes según las directrices para adultos. Para obtener más información, consultar la sección
Información sobre los estadios del melanoma en Tratamiento del melanoma. Por el contrario, los pacientes con melanoma spitzoide tienen un riesgo bajo de recidiva y desenlaces clínicos excelentes, por lo tanto no necesitan una evaluación radiográfica extensa en el momento del diagnóstico ni durante el seguimiento.[12 ]
Referencias:
- Berk DR, LaBuz E, Dadras SS, et al.: Melanoma and melanocytic tumors of uncertain malignant potential in children, adolescents and young adults--the Stanford experience 1995-2008. Pediatr Dermatol 27 (3): 244-54, 2010 May-Jun.
- Cerroni L, Barnhill R, Elder D, et al.: Melanocytic tumors of uncertain malignant potential: results of a tutorial held at the XXIX Symposium of the International Society of Dermatopathology in Graz, October 2008. Am J Surg Pathol 34 (3): 314-26, 2010.
- Cordoro KM, Gupta D, Frieden IJ, et al.: Pediatric melanoma: results of a large cohort study and proposal for modified ABCD detection criteria for children. J Am Acad Dermatol 68 (6): 913-25, 2013.
- Ferrari A, Lopez Almaraz R, Reguerre Y, et al.: Cutaneous melanoma in children and adolescents: The EXPeRT/PARTNER diagnostic and therapeutic recommendations. Pediatr Blood Cancer 68 (Suppl 4): e28992, 2021.
- Shah NC, Gerstle JT, Stuart M, et al.: Use of sentinel lymph node biopsy and high-dose interferon in pediatric patients with high-risk melanoma: the Hospital for Sick Children experience. J Pediatr Hematol Oncol 28 (8): 496-500, 2006.
- Kayton ML, La Quaglia MP: Sentinel node biopsy for melanocytic tumors in children. Semin Diagn Pathol 25 (2): 95-9, 2008.
- Swetter SM, Thompson JA, Albertini MR, et al.: NCCN Guidelines® Insights: Melanoma: Cutaneous, Version 2.2021. J Natl Compr Canc Netw 19 (4): 364-376, 2021.
- Ariyan CE, Coit DG: Clinical aspects of sentinel lymph node biopsy in melanoma. Semin Diagn Pathol 25 (2): 86-94, 2008.
- Pacella SJ, Lowe L, Bradford C, et al.: The utility of sentinel lymph node biopsy in head and neck melanoma in the pediatric population. Plast Reconstr Surg 112 (5): 1257-65, 2003.
- Lallas A, Kyrgidis A, Ferrara G, et al.: Atypical Spitz tumours and sentinel lymph node biopsy: a systematic review. Lancet Oncol 15 (4): e178-83, 2014.
- Lee S, Barnhill RL, Dummer R, et al.: TERT Promoter Mutations Are Predictive of Aggressive Clinical Behavior in Patients with Spitzoid Melanocytic Neoplasms. Sci Rep 5: 11200, 2015.
- Halalsheh H, Kaste SC, Navid F, et al.: The role of routine imaging in pediatric cutaneous melanoma. Pediatr Blood Cancer 65 (12): e27412, 2018.
Características moleculares
El diagnóstico exacto de las lesiones melanocíticas en pediatría es fundamental para la estratificación del riesgo adecuada y la planificación del tratamiento.
Las afecciones relacionadas con el melanoma que tienen potencial maligno y surgen en la población pediátrica se clasifican en tres grupos generales:[
- Tumores melanocíticos spitzoides, que incluyen desde los tumores de Spitz atípicos hasta los melanomas spitzoides.
- Melanoma en adolescentes mayores que comparte características con el melanoma en adultos (es decir, melanoma convencional).
- Nevo melanocítico congénito gigante.
Las lesiones clasificadas como lesiones de Spitz representan un reto diagnóstico y la evaluación morfológica sola tiene grandes limitaciones y exhibe un consenso bajo entre diferentes observadores expertos.[
En las lesiones melanocíticas se han notificado alteraciones genómicas que comprometen varios genes. Las características de cada tipo de tumor se resumen en el
- El panorama genómico de los melanomas spitzoides se caracteriza por fusiones que afectan varios genes de cinasas, entre ellos, RET, MAP3K8, ROS1, NTRK1, ALK, MET y BRAF.[
3 ,4 ,5 ,6 ] Estos genes de fusión se han notificado en cerca del 50 % de los casos y se presentan de manera mutuamente excluyente.[1 ,4 ] - En un análisis retrospectivo de tumores spitzoides de 49 pacientes, se usó secuenciación del genoma completo y del transcriptoma (RNA-Seq) y se encontraron fusiones en el marco de lectura o interrupción por truncamiento del extremo C de MAP3K8 en el 33 % de los casos.[
6 ] - Las variantes en el promotor de TERT son poco frecuentes en las lesiones melanocíticas spitzoides y solo se observaron en 4 de 56 pacientes evaluados en una serie. No obstante, los 4 casos con variantes en el promotor de TERT presentaron metástasis hematógenas y murieron. Este hallazgo respalda el potencial de las variantes en el promotor de TERT como factor predictivo del comportamiento clínico maligno de las neoplasias melanocíticas spitzoides en la niñez, pero se necesitan más estudios para definir la función del estado del promotor de TERT natural como factor predictivo del comportamiento clínico en pacientes con tumores spitzoides en el sitio primario.[
4 ] - En un análisis retrospectivo de 352 casos de nevos de Spitz se identificaron oncoiniciadores en el 76 % de los pacientes.[
7 ] Ninguna característica microscópica permitió predecir de manera confiable los casos que presentaban sobrexpresión de ROS1 y NTRK1. Por el contrario, la configuración plexiforme se asoció con sobrexpresión de ALK. La variante de pseudo-schwannoma fue muy sugestiva de casos con reordenamiento de NTRK3. Un tumor atípico maligno, la atipia celular grave y la pérdida de p16 se asociaron con reordenamientos del gen MAP3K8. La arquitectura en láminas y la fibrosis estromal marcada se asociaron con fusiones en BRAF.
En otro estudio, 128 lesiones se clasificaron como tumores de Spitz de acuerdo a sus características morfológicas (80 tumores de Spitz, 26 melanomas de Spitz, 22 melanomas con características de tipo Spitz).[
- Se presentaron fusiones o truncamientos de cinasas en el 81 % de los casos de tumores de Spitz y en el 77 % de los casos de melanomas de Spitz. En comparación, el 84 % de los melanomas con características de tipo Spitz tenían variantes de BRAF, NRAS o NF1, y el 61 % de estos casos también exhibían variantes en el promotor de TERT.
- Entre los pacientes del grupo de tumores de Spitz cuyos melanomas recidivaron, 1 paciente con variante BRAF V600E y variante en el promotor de TERT presentó una recidiva a distancia y murió. Otro paciente con una fusión de MAP3K8 tuvo una recidiva local.
- De los pacientes con melanoma de Spitz, 2 presentaron recidivas, ambos tenían variantes BRAF V600E.
- Los 3 pacientes del grupo de melanoma con características spitzoides que presentaron recidiva tenían una variante en BRAF o en NRAS y variantes simultáneas en el promotor de TERT.
- Después de reclasificar a estos pacientes según sus características clínicas y genómicas, y de añadir las variantes de BRAF o NRAS dentro de la categoría de melanoma con características de tipo Spitz, se pudo observar una diferencia significativa en las tasas de supervivencia sin recidiva entre los grupos con tumores de Spitz. Estos hallazgos indican que la incorporación de las características genómicas permite mejorar la clasificación de las lesiones.
Melanoma convencional o clásico. El panorama genómico del melanoma convencional en la niñez se caracteriza por muchas de las alteraciones genómicas que se encuentran en el melanoma de adultos.[
Nevos melanocíticos congénitos gigantes. Se informó que los nevos melanocíticos congénitos gigantes tienen variantes activadoras NRASQ61 sin otras variantes recurrentes.[
Al integrar el análisis genómico en la evaluación de las lesiones melanocíticas infantiles es posible optimizar la exactitud del diagnóstico y obtener información pronóstica de importancia para el médico tratante. En un registro prospectivo de 70 pacientes con lesiones melanocíticas infantiles, la evaluación clinicopatológica y genómica integral optimizó el diagnóstico patológico y mejoró la capacidad de predecir desenlaces clínicos en estos pacientes.[
- Tumor de Spitz atípico o melanoma de Spitz.
- Los pacientes con tumores de Spitz atípicos o melanomas de Spitz eran más jóvenes y por lo general los tumores estaban en las extremidades.
- Las lesiones genómicas de estos pacientes se caracterizaron por fusiones de cinasas que afectaron con mayor frecuencia los genes MAP3K8 y ALK.
- A pesar de que el 62 % de los pacientes a los que se les tomaron muestras de ganglios linfáticos tenía enfermedad ganglionar, ninguno presentó metástasis a distancia y 2 tuvieron recidivas locorregionales.
- De los 33 pacientes analizados, ninguno presentó variantes en el promotor de TERT. Sin embargo, 15 pacientes tuvieron deleciones de CDKN2A. Estos hallazgos indican que las variantes en el promotor de TERT quizás sean factores pronósticos más acertados del comportamiento clínico agresivo (formación de metástasis) de estas lesiones.
- Melanoma convencional o clásico.
- Los pacientes con melanoma convencional (n = 17) eran mayores y con más frecuencia sus tumores se encontraban en el cuero cabelludo o el torso.
- De 12 pacientes, 7 presentaron compromiso de ganglio linfático centinela.
- De 17 pacientes, 11 presentaron variantes BRAF V600E.
- De 16 pacientes, 7 tenían variantes en el promotor de TERT y 3 de estos pacientes murieron.
- Nevos gigantes.
- De los 4 pacientes con melanoma que surgió a partir de un nevo gigante, todos tenían variantes NRASQ61 y fallecieron por la enfermedad.
| Tumor | Gen afectado |
|---|---|
| Melanoma | BRAF,NRAS,KIT,NF1 |
| Melanoma de Spitz | Fusión de cinasas (RET,ROS,MET,ALK,BRAF,MAP3K8NTRK1); pérdida deBAP1en presencia de una variante enBRAF |
| Nevo de Spitz | HRAS;BRAFyNRAS(infrecuentes); fusiones de cinasas (ROS,ALK,NTRK1,BRAF,RET,MAP3K8) |
| Nevo adquirido | BRAF |
| Nevo displásico | BRAF,NRAS |
| Nevo azul | GNAQ |
| Melanoma ocular | GNAQ |
| Nevos congénitos | NRAS |
Referencias:
- Lu C, Zhang J, Nagahawatte P, et al.: The genomic landscape of childhood and adolescent melanoma. J Invest Dermatol 135 (3): 816-23, 2015.
- Gerami P, Busam K, Cochran A, et al.: Histomorphologic assessment and interobserver diagnostic reproducibility of atypical spitzoid melanocytic neoplasms with long-term follow-up. Am J Surg Pathol 38 (7): 934-40, 2014.
- Wiesner T, He J, Yelensky R, et al.: Kinase fusions are frequent in Spitz tumours and spitzoid melanomas. Nat Commun 5: 3116, 2014.
- Lee S, Barnhill RL, Dummer R, et al.: TERT Promoter Mutations Are Predictive of Aggressive Clinical Behavior in Patients with Spitzoid Melanocytic Neoplasms. Sci Rep 5: 11200, 2015.
- Yeh I, Botton T, Talevich E, et al.: Activating MET kinase rearrangements in melanoma and Spitz tumours. Nat Commun 6: 7174, 2015.
- Newman S, Fan L, Pribnow A, et al.: Clinical genome sequencing uncovers potentially targetable truncations and fusions of MAP3K8 in spitzoid and other melanomas. Nat Med 25 (4): 597-602, 2019.
- Kervarrec T, Pissaloux D, Tirode F, et al.: Morphologic features in a series of 352 Spitz melanocytic proliferations help predict their oncogenic drivers. Virchows Arch 480 (2): 369-382, 2022.
- Quan VL, Zhang B, Zhang Y, et al.: Integrating Next-Generation Sequencing with Morphology Improves Prognostic and Biologic Classification of Spitz Neoplasms. J Invest Dermatol 140 (8): 1599-1608, 2020.
- Wilmott JS, Johansson PA, Newell F, et al.: Whole genome sequencing of melanomas in adolescent and young adults reveals distinct mutation landscapes and the potential role of germline variants in disease susceptibility. Int J Cancer 144 (5): 1049-1060, 2019.
- Charbel C, Fontaine RH, Malouf GG, et al.: NRAS mutation is the sole recurrent somatic mutation in large congenital melanocytic nevi. J Invest Dermatol 134 (4): 1067-74, 2014.
- Kinsler VA, Thomas AC, Ishida M, et al.: Multiple congenital melanocytic nevi and neurocutaneous melanosis are caused by postzygotic mutations in codon 61 of NRAS. J Invest Dermatol 133 (9): 2229-36, 2013.
- Pappo AS, McPherson V, Pan H, et al.: A prospective, comprehensive registry that integrates the molecular analysis of pediatric and adolescent melanocytic lesions. Cancer 127 (20): 3825-3831, 2021.
Pronóstico y factores pronósticos
Los niños y adolescentes con melanoma por lo general tienen un desenlace favorable. En el
| Edad (años) | Tasa de supervivencia relativa a 5 años (%) | Límite inferior del intervalo de confianza de 95 % | Límite superior del intervalo de confianza de 95 % |
|---|---|---|---|
| a Adaptación de National Childhood Cancer Registry. NCCR*Explorer: An interactive website for NCCR cancer statistics [Internet]. Instituto Nacional del Cáncer; sept. 7 de 2023. [actualizado el 8 de sept. de 2023; citado el 12 de agosto de 2024]. Disponible en: https://nccrexplorer.ccdi.cancer.gov. | |||
| <1 | 85 | 63 | 94 |
| 1–4 | 83 | 71 | 90 |
| 5–9 | 99 | 95 | 100 |
| 10–14 | 95 | 90 | 97 |
| 15–19 | 97 | 95 | 99 |
El melanoma infantil comparte muchas características con el melanoma en adultos, y el pronóstico depende del estadio de la enfermedad.[
El desenlace de los pacientes con enfermedad ganglionar es intermedio, se anticipa que cerca del 60 % sobrevivirá a largo plazo.[
Los siguientes elementos suelen ser comunes en niños menores de 10 años que tienen melanoma:[
- Características de pronóstico precario.
- Raza diferente a la blanca.
- Tumores primarios en la cabeza y el cuello.
- Lesiones primarias más gruesas.
- Incidencia más alta de características morfológicas spitzoides, invasión vascular y metástasis ganglionares.
- Síndromes de predisposición al melanoma.
Se ha generalizado el uso de la biopsia de ganglio linfático centinela para la estadificación del melanoma infantil. El grosor del tumor primario y la presencia de ulceración se correlacionan con una incidencia alta de compromiso ganglionar.[
- Los pacientes más jóvenes presentan una incidencia más alta de compromiso ganglionar; pero este hallazgo no afecta significativamente los desenlaces clínicos.[
7 ,9 ] - En otra serie de melanoma infantil, una incidencia más alta de compromiso ganglionar no afectó la supervivencia.[
10 ,11 ,12 ] - En un estudio de cohorte retrospectivo de la National Cancer Database, se revisaron todos los registros de los pacientes con un diagnóstico inicial de melanoma entre 1998 y 2011. Los datos se obtuvieron de historias clínicas, informes quirúrgicos, e informes de patología y no se sometieron a revisión central. Se identificaron 350 928 pacientes con información adecuada; 306 pacientes tenían entre 1 y 10 años (niños), y 3659 pacientes tenían entre 11 y 20 años (adolescentes).[
13 ]- Los niños presentaron una supervivencia general (SG) más larga que los adolescentes (cociente de riesgos instantáneos [CRI], 0,50; intervalo de confianza [IC] 95 %, 0,25–0,98) y los adultos mayores de 20 años (CRI, 0,11; IC 95 %, 0,06–0,21).
- Los adolescentes tuvieron una SG más larga que los adultos.
- No se encontraron diferencias en la SG entre los niños con compromiso ganglionar y sin este.
- En los niños, la biopsia de ganglio linfático centinela y la disección ganglionar completa no se relacionaron con un aumento de la SG.
- En los adolescentes, el compromiso ganglionar fue un factor de pronóstico adverso significativo (CRI, 4,82; IC 95 %, 3,38–6,87).
La relación entre el grosor de la lesión y el desenlace clínico del melanoma infantil es objeto de controversia.[
Referencias:
- National Cancer Institute: NCCR*Explorer: An interactive website for NCCR cancer statistics. Bethesda, MD: National Cancer Institute.
Available online . Last accessed February 25, 2025. - Paradela S, Fonseca E, Pita-Fernández S, et al.: Prognostic factors for melanoma in children and adolescents: a clinicopathologic, single-center study of 137 Patients. Cancer 116 (18): 4334-44, 2010.
- Wong JR, Harris JK, Rodriguez-Galindo C, et al.: Incidence of childhood and adolescent melanoma in the United States: 1973-2009. Pediatrics 131 (5): 846-54, 2013.
- Strouse JJ, Fears TR, Tucker MA, et al.: Pediatric melanoma: risk factor and survival analysis of the surveillance, epidemiology and end results database. J Clin Oncol 23 (21): 4735-41, 2005.
- Brecht IB, Garbe C, Gefeller O, et al.: 443 paediatric cases of malignant melanoma registered with the German Central Malignant Melanoma Registry between 1983 and 2011. Eur J Cancer 51 (7): 861-8, 2015.
- Lange JR, Palis BE, Chang DC, et al.: Melanoma in children and teenagers: an analysis of patients from the National Cancer Data Base. J Clin Oncol 25 (11): 1363-8, 2007.
- Moore-Olufemi S, Herzog C, Warneke C, et al.: Outcomes in pediatric melanoma: comparing prepubertal to adolescent pediatric patients. Ann Surg 253 (6): 1211-5, 2011.
- Mu E, Lange JR, Strouse JJ: Comparison of the use and results of sentinel lymph node biopsy in children and young adults with melanoma. Cancer 118 (10): 2700-7, 2012.
- Balch CM, Soong SJ, Gershenwald JE, et al.: Age as a prognostic factor in patients with localized melanoma and regional metastases. Ann Surg Oncol 20 (12): 3961-8, 2013.
- Gibbs P, Moore A, Robinson W, et al.: Pediatric melanoma: are recent advances in the management of adult melanoma relevant to the pediatric population. J Pediatr Hematol Oncol 22 (5): 428-32, 2000 Sep-Oct.
- Livestro DP, Kaine EM, Michaelson JS, et al.: Melanoma in the young: differences and similarities with adult melanoma: a case-matched controlled analysis. Cancer 110 (3): 614-24, 2007.
- Han D, Zager JS, Han G, et al.: The unique clinical characteristics of melanoma diagnosed in children. Ann Surg Oncol 19 (12): 3888-95, 2012.
- Lorimer PD, White RL, Walsh K, et al.: Pediatric and Adolescent Melanoma: A National Cancer Data Base Update. Ann Surg Oncol 23 (12): 4058-4066, 2016.
- Rao BN, Hayes FA, Pratt CB, et al.: Malignant melanoma in children: its management and prognosis. J Pediatr Surg 25 (2): 198-203, 1990.
- Aldrink JH, Selim MA, Diesen DL, et al.: Pediatric melanoma: a single-institution experience of 150 patients. J Pediatr Surg 44 (8): 1514-21, 2009.
- Tcheung WJ, Marcello JE, Puri PK, et al.: Evaluation of 39 cases of pediatric cutaneous head and neck melanoma. J Am Acad Dermatol 65 (2): e37-42, 2011.
- Ferrari A, Bisogno G, Cecchetto G, et al.: Cutaneous melanoma in children and adolescents: the Italian rare tumors in pediatric age project experience. J Pediatr 164 (2): 376-82.e1-2, 2014.
- Stanelle EJ, Busam KJ, Rich BS, et al.: Early-stage non-Spitzoid cutaneous melanoma in patients younger than 22 years of age at diagnosis: long-term follow-up and survival analysis. J Pediatr Surg 50 (6): 1019-23, 2015.
- Lohmann CM, Coit DG, Brady MS, et al.: Sentinel lymph node biopsy in patients with diagnostically controversial spitzoid melanocytic tumors. Am J Surg Pathol 26 (1): 47-55, 2002.
- Su LD, Fullen DR, Sondak VK, et al.: Sentinel lymph node biopsy for patients with problematic spitzoid melanocytic lesions: a report on 18 patients. Cancer 97 (2): 499-507, 2003.
Consideraciones especiales para el tratamiento de niños con cáncer
El cáncer en niños y adolescentes es raro, aunque desde 1975 se ha observado un aumento gradual de la incidencia general.[
- Médicos de atención primaria.
- Cirujanos pediatras.
- Patólogos.
- Radioncólogo pediatras.
- Oncólogos y hematólogos pediatras.
- Oftalmólogos.
- Especialistas en rehabilitación.
- Enfermeros de oncología pediátrica.
- Trabajadores o asistentes sociales.
- Profesionales de la vida infantil.
- Psicólogos.
- Nutricionistas y dietistas.
Para obtener información específica sobre los cuidados médicos de apoyo para niños y adolescentes con cáncer, consultar los resúmenes de
La American Academy of Pediatrics estableció pautas para los centros de oncología pediátrica y su función en el tratamiento de los pacientes con cáncer infantil.[
Se han logrado mejoras notables en la supervivencia de niños y adolescentes con cáncer. Entre 1975 y 2020, la mortalidad por cáncer infantil disminuyó en más del 50 %.[
El cáncer infantil (cáncer en edad pediátrica) es una enfermedad rara con cerca de 15 000 casos anuales diagnosticados antes de los 20 años de edad en los Estados Unidos.[
La designación de un tumor raro es diferente entre los grupos pediátricos y de adultos. En el caso de los adultos, se considera que un cáncer es raro cuando su incidencia anual es inferior a 6 casos por 100 000 personas. Representan hasta el 24 % de los cánceres diagnosticados en la Unión Europea y alrededor del 20 % de los cánceres diagnosticados en los Estados Unidos.[
- En una iniciativa conjunta de la European Union Joint Action on Rare Cancers y el European Cooperative Study Group for Rare Pediatric Cancers se estimó que el 11 % de todos los cánceres en pacientes menores de 20 años se podrían clasificar como muy raros. Este grupo de consenso definió los cánceres muy raros como los cánceres con incidencia anual inferior a 2 casos por millón de personas. Sin embargo, también se incluyen en este grupo de tumores muy raros otros 3 tipos histológicos (carcinoma de tiroides, melanoma y cáncer de testículo) con incidencias superiores a 2 casos por millón de personas, porque se cuenta con poco conocimiento y experiencia sobre el tratamiento de estos tumores.[
9 ] - El Children's Oncology Group (COG) define los cánceres raros en pediatría según la lista del subgrupo XI de la International Classification of Childhood Cancer, en la que se incluyen los cánceres de tiroides, los cánceres de piel melanoma y no melanoma, además de los múltiples tipos de carcinomas (por ejemplo, los carcinomas de corteza suprarrenal, los carcinomas de nasofaringe y la mayoría de los carcinomas de tipo adulto, como los cánceres de mama, los cánceres colorrectales, etc.).[
10 ] Estos cánceres representan casi el 5 % de aquellos diagnosticados entre los 0 y 14 años de edad y casi el 27 % de los que se diagnostican entre los 15 a 19 años de edad.[4 ]La mayoría de los cánceres del subgrupo XI son melanomas o cánceres de tiroides, mientras que otros tipos de cáncer solo representan el 2 % de los cánceres diagnosticados entre los 0 y 14 años de edad y el 9,3 % de los cánceres entre los 15 y 19 años de edad.
Estudiar estos cánceres raros es un reto por el número bajo de pacientes con cualquier diagnóstico individual, el predominio de estos cánceres raros en adolescentes y la carencia de ensayos clínicos con adolescentes que tienen estos cánceres.
También es posible obtener información sobre estos tumores en fuentes relacionadas con el cáncer en adultos, por ejemplo, en
Referencias:
- Smith MA, Seibel NL, Altekruse SF, et al.: Outcomes for children and adolescents with cancer: challenges for the twenty-first century. J Clin Oncol 28 (15): 2625-34, 2010.
- American Academy of Pediatrics: Standards for pediatric cancer centers. Pediatrics 134 (2): 410-4, 2014.
Also available online . Last accessed February 25, 2025. - Smith MA, Altekruse SF, Adamson PC, et al.: Declining childhood and adolescent cancer mortality. Cancer 120 (16): 2497-506, 2014.
- National Cancer Institute: NCCR*Explorer: An interactive website for NCCR cancer statistics. Bethesda, MD: National Cancer Institute.
Available online . Last accessed February 25, 2025. - Surveillance Research Program, National Cancer Institute: SEER*Explorer: An interactive website for SEER cancer statistics. Bethesda, MD: National Cancer Institute.
Available online . Last accessed December 30, 2024. - Ward E, DeSantis C, Robbins A, et al.: Childhood and adolescent cancer statistics, 2014. CA Cancer J Clin 64 (2): 83-103, 2014 Mar-Apr.
- Gatta G, Capocaccia R, Botta L, et al.: Burden and centralised treatment in Europe of rare tumours: results of RARECAREnet-a population-based study. Lancet Oncol 18 (8): 1022-1039, 2017.
- DeSantis CE, Kramer JL, Jemal A: The burden of rare cancers in the United States. CA Cancer J Clin 67 (4): 261-272, 2017.
- Ferrari A, Brecht IB, Gatta G, et al.: Defining and listing very rare cancers of paediatric age: consensus of the Joint Action on Rare Cancers in cooperation with the European Cooperative Study Group for Pediatric Rare Tumors. Eur J Cancer 110: 120-126, 2019.
- Pappo AS, Krailo M, Chen Z, et al.: Infrequent tumor initiative of the Children's Oncology Group: initial lessons learned and their impact on future plans. J Clin Oncol 28 (33): 5011-6, 2010.
Tratamiento del melanoma infantil
El European Cooperative Study Group for Pediatric Rare Tumors que es parte del proyecto PARTNER (Paediatric Rare Tumours Network - European Registry) publicó recomendaciones para el diagnóstico y tratamiento de niños y adolescentes con melanoma cutáneo. Algunas de estas recomendaciones se han incorporado y resumido en las secciones que siguen.[
Las opciones de tratamiento del melanoma infantil son las siguientes:
-
Cirugía y, en determinados casos, biopsia de ganglio linfático centinela con disección ganglionar. -
Inhibidores de puntos de control inmunitario o inhibidores de BRAF/MEK .
Cirugía
La cirugía es el tratamiento preferido para los pacientes con melanoma localizado. Las directrices actuales recomiendan los siguientes márgenes de resección:
- 0,5 cm para el melanoma in situ.
- 1 cm para el melanoma de menos de 1 mm de grosor.
- 1 cm a 2 cm para el melanoma de 1,01 mm a 2 mm de grosor.
- 2 cm para un tumor de más de 2 mm de grosor.
Se deberá considerar una biopsia de ganglio linfático centinela en los pacientes con lesiones delgadas (≤1 mm) y ulceración, tasa mitótica mayor de 1/mm2, edad temprana, y lesiones de más de 1 mm, con características adversas o sin ellas. Los pacientes más jóvenes tienen una incidencia más alta de compromiso de ganglio linfático centinela, y esta característica afecta de manera adversa los desenlaces clínicos.[
Si hay compromiso del ganglio linfático centinela, se deberá analizar la opción de una disección ganglionar completa. En un ensayo de adultos participaron 1934 pacientes con compromiso de ganglio linfático centinela detectado mediante prueba inmunohistoquímica o reacción en cadena de la polimerasa. Los pacientes se asignaron al azar a someterse a una disección ganglionar completa u observación. La tasa de supervivencia a 3 años específica para el melanoma fue similar en ambos grupos (86 %), mientras que la tasa de supervivencia sin enfermedad (SSE) fue un poco más alta en el grupo de disección (68 vs. 63 %; P = 0,05). Esta ventaja de la SSE se relacionó con una disminución en la tasa de recidiva ganglionar debido a que no hubo diferencia en las tasas de supervivencia sin metástasis a distancia. Se desconoce la forma en que estos resultados afectarán la determinación futura del tratamiento quirúrgico del melanoma durante la infancia y adolescencia.[
Inhibidor de puntos de control inmunitario e inhibidores de BRAF o MEK
Las terapias dirigidas y la inmunoterapia que han demostrado eficacia para los adultos con melanoma deberían probarse en pacientes pediátricos con melanoma convencional y con enfermedad metastásica, recidivante o progresiva.
Evidencia (terapia dirigida e inmunoterapia):
- En un ensayo de fase I de ipilimumab en niños y adolescentes, que recibieron una dosis de 5 mg/kg o 10 mg/kg cada 3 semanas durante 4 ciclos, se inscribieron 12 pacientes con melanoma.[
5 ]- Un paciente presentó enfermedad estable prolongada.
- Este tratamiento se relacionó con un perfil de toxicidad similar al que se observó en los adultos.
- En un estudio de fase II de ipilimumab en adolescentes con melanoma no se logró la meta de inscripción y se cerró. No obstante, en pacientes de 12 a 17 años con melanoma se notificó actividad de este medicamento y un perfil de inocuidad similar al de adultos.[
6 ][Nivel de evidencia B4]- Después de 1 año, 3 de 4 pacientes que recibieron 3 mg/kg, y 5 de 8 pacientes que recibieron 10 mg/kg seguían vivos.
- Se observó respuesta parcial en 2 pacientes que recibieron 10 mg/kg, y enfermedad estable en 1 paciente que recibió 3 mg/kg.
- En los adultos con melanoma cutáneo en estadio III que se extirpó por completo, se demostró un aumento de la SSE y la supervivencia general con la administración de ipilimumab en dosis de 10 mg/kg cada 3 semanas durante 4 dosis, seguidas de 1 dosis cada 3 meses hasta un máximo de 3 años. Este régimen causó poca alteración de la calidad de vida relacionada con la salud.
- En un ensayo de fase I/II de nivolumab en niños y adultos con tumores sólidos o linfoma en recaída o resistentes al tratamiento, se administró a los pacientes una dosis de 3 mg/kg cada 14 días.[
7 ]- El único paciente con melanoma no respondió al tratamiento.
- En un ensayo de fase I/II sin anonimato y de un solo grupo de pembrolizumab en pacientes pediátricos con melanoma en estadio avanzado, o con tumores sólidos o linfoma resistentes al tratamiento, en recaída, en estadio avanzado o positivos para el ligando 1 de muerte celular programada (PD-L1), se notificó lo siguiente:[
8 ]- Se inscribieron 8 pacientes con melanoma y no se observaron respuestas en estos pacientes.
- De estos pacientes, 5 eran negativos para PD-L1.
- El Children's Oncology Group llevó adelante un ensayo de fase I/II de ipilimumab y nivolumab en 55 niños y adultos jóvenes con tumores sólidos resistentes al tratamiento o recidivantes.[
9 ]- En el estudio se determinó una dosis recomendada para la fase II de 3 mg/kg para el nivolumab y de 1 mg/kg para el ipilimumab.
- En el ensayo no se incluyeron pacientes con melanoma. Sin embargo, se observaron respuestas parciales en un paciente con rabdomiosarcoma y en un paciente con sarcoma de Ewing.
- El dabrafenib y el trametinib se estudiaron en dos ensayos de pacientes pediátricos con gliomas de grado bajo que albergaban alteraciones BRAF V600. La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó esta combinación para dicha indicación.[
10 ,11 ] La FDA también aprobó esta indicación para el tratamiento de pacientes con melanoma.
No se han realizado ensayos específicos para el tratamiento de pacientes pediátricos con melanoma. Sin embargo, la FDA aprobó las siguientes terapias dirigidas e inmunoterapias para pacientes pediátricos y adolescentes con melanoma a partir de los estudios en poblaciones de adultos que incluyeron o no la participación de pacientes en edad pediátrica:
- A partir de los buenos resultados de dos ensayos clínicos aleatorizados, la FDA aprobó el uso de pembrolizumab adyuvante para el tratamiento de pacientes de 12 años o más con melanoma resecado en estadio IIb, IIc y III.[
12 ,13 ] - A partir de los buenos resultados de dos ensayos clínicos aleatorizados, la FDA aprobó el uso de nivolumab adyuvante para el tratamiento de pacientes de 12 años o más con melanoma resecado en estadio IIb a IV.[
14 ,15 ] - A partir de los buenos resultados de un ensayo clínico aleatorizado realizado en adultos, la FDA aprobó el uso de nivolumab e ipilimumab para el tratamiento de niños de 12 años o más con melanoma irresecable o metastásico.[
16 ] - A partir de los buenos resultados de un ensayo clínico aleatorizado, la FDA aprobó el uso de nivolumab con relatlimab para el tratamiento de niños de 12 año o más con melanoma irresecable o metastásico.[
17 ] - Si bien no se han realizado ensayos clínicos prospectivos con inhibidores de BRAF o MEK en niños y adolescentes con melanoma, en dos estudios de adultos se observó que la combinación adyuvante de dabrafenib y trametinib produce un riesgo significativamente más bajo de recidiva en pacientes con melanoma en estadio III resecado mediante cirugía y en pacientes con melanoma metastásico que alberga la alteración BRAF V600 y que no recibieron tratamiento.[
18 ,19 ] La FDA otorgó la aprobación acelerada a esta combinación de medicamentos para el tratamiento de pacientes con melanoma irresecable o metastásico que alberga variantes BRAF V600E o V600K y para el tratamiento adyuvante de pacientes con melanoma que alberga variantes BRAF V600E o V600K.
Para obtener más información, consultar
Referencias:
- Ferrari A, Lopez Almaraz R, Reguerre Y, et al.: Cutaneous melanoma in children and adolescents: The EXPeRT/PARTNER diagnostic and therapeutic recommendations. Pediatr Blood Cancer 68 (Suppl 4): e28992, 2021.
- Mu E, Lange JR, Strouse JJ: Comparison of the use and results of sentinel lymph node biopsy in children and young adults with melanoma. Cancer 118 (10): 2700-7, 2012.
- Han D, Zager JS, Han G, et al.: The unique clinical characteristics of melanoma diagnosed in children. Ann Surg Oncol 19 (12): 3888-95, 2012.
- Eggermont AM, Chiarion-Sileni V, Grob JJ, et al.: Prolonged Survival in Stage III Melanoma with Ipilimumab Adjuvant Therapy. N Engl J Med 375 (19): 1845-1855, 2016.
- Merchant MS, Wright M, Baird K, et al.: Phase I Clinical Trial of Ipilimumab in Pediatric Patients with Advanced Solid Tumors. Clin Cancer Res 22 (6): 1364-70, 2016.
- Geoerger B, Bergeron C, Gore L, et al.: Phase II study of ipilimumab in adolescents with unresectable stage III or IV malignant melanoma. Eur J Cancer 86: 358-363, 2017.
- Davis KL, Fox E, Merchant MS, et al.: Nivolumab in children and young adults with relapsed or refractory solid tumours or lymphoma (ADVL1412): a multicentre, open-label, single-arm, phase 1-2 trial. Lancet Oncol 21 (4): 541-550, 2020.
- Geoerger B, Kang HJ, Yalon-Oren M, et al.: Pembrolizumab in paediatric patients with advanced melanoma or a PD-L1-positive, advanced, relapsed, or refractory solid tumour or lymphoma (KEYNOTE-051): interim analysis of an open-label, single-arm, phase 1-2 trial. Lancet Oncol 21 (1): 121-133, 2020.
- Davis KL, Fox E, Isikwei E, et al.: A Phase I/II Trial of Nivolumab plus Ipilimumab in Children and Young Adults with Relapsed/Refractory Solid Tumors: A Children's Oncology Group Study ADVL1412. Clin Cancer Res 28 (23): 5088-5097, 2022.
- Hargrave DR, Bouffet E, Tabori U, et al.: Efficacy and Safety of Dabrafenib in Pediatric Patients with BRAF V600 Mutation-Positive Relapsed or Refractory Low-Grade Glioma: Results from a Phase I/IIa Study. Clin Cancer Res 25 (24): 7303-7311, 2019.
- Bouffet E, Hansford JR, Garrè ML, et al.: Dabrafenib plus Trametinib in Pediatric Glioma with BRAF V600 Mutations. N Engl J Med 389 (12): 1108-1120, 2023.
- Eggermont AMM, Blank CU, Mandala M, et al.: Adjuvant Pembrolizumab versus Placebo in Resected Stage III Melanoma. N Engl J Med 378 (19): 1789-1801, 2018.
- Luke JJ, Rutkowski P, Queirolo P, et al.: Pembrolizumab versus placebo as adjuvant therapy in completely resected stage IIB or IIC melanoma (KEYNOTE-716): a randomised, double-blind, phase 3 trial. Lancet 399 (10336): 1718-1729, 2022.
- Kirkwood JM, Del Vecchio M, Weber J, et al.: Adjuvant nivolumab in resected stage IIB/C melanoma: primary results from the randomized, phase 3 CheckMate 76K trial. Nat Med 29 (11): 2835-2843, 2023.
- Weber J, Mandala M, Del Vecchio M, et al.: Adjuvant Nivolumab versus Ipilimumab in Resected Stage III or IV Melanoma. N Engl J Med 377 (19): 1824-1835, 2017.
- Wolchok JD, Chiarion-Sileni V, Gonzalez R, et al.: Overall Survival with Combined Nivolumab and Ipilimumab in Advanced Melanoma. N Engl J Med 377 (14): 1345-1356, 2017.
- Tawbi HA, Schadendorf D, Lipson EJ, et al.: Relatlimab and Nivolumab versus Nivolumab in Untreated Advanced Melanoma. N Engl J Med 386 (1): 24-34, 2022.
- Robert C, Karaszewska B, Schachter J, et al.: Improved overall survival in melanoma with combined dabrafenib and trametinib. N Engl J Med 372 (1): 30-9, 2015.
- Long GV, Hauschild A, Santinami M, et al.: Adjuvant Dabrafenib plus Trametinib in Stage III BRAF-Mutated Melanoma. N Engl J Med 377 (19): 1813-1823, 2017.
Opciones de tratamiento en evaluación clínica para el melanoma infantil
La información en inglés sobre los ensayos clínicos patrocinados por el Instituto Nacional del Cáncer (NCI) se encuentra en el
A continuación, se presenta un ejemplo de un ensayo clínico nacional o institucional en curso:
- NCT02332668 (A Study of Pembrolizumab [MK-3475] in Pediatric Participants With Advanced Melanoma or Advanced, Relapsed, or Refractory PD-L1-Positive Solid Tumors or Lymphoma [MK-3475-051/KEYNOTE-051]): este es un estudio en dos partes de pembrolizumab en niños con melanoma en estadio avanzado, o un tumor sólido o linfoma en estadio avanzado, en recaída o resistente al tratamiento positivo para el ligando 1 de muerte celular programada (PD-L1). En la parte 1 se intentará encontrar la dosis máxima tolerada o administrada, confirmar la dosis, y determinar la dosis recomendada de fase II para el tratamiento con pembrolizumab. En la parte 2 se evaluarán con mayor profundidad la inocuidad y la eficacia de la dosis de la fase II recomendada para pacientes pediátricos.
Actualizaciones más recientes a este resumen (01 / 17 / 2025)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes introducidos en este resumen a partir de la fecha arriba indicada.
Este resumen fue objeto de revisión integral.
El
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre el tratamiento del melanoma infantil. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Tratamiento del melanoma infantil son:
- Denise Adams, MD (Children's Hospital Boston)
- Karen J. Marcus, MD, FACR (Dana-Farber of Boston Children's Cancer Center and Blood Disorders Harvard Medical School)
- William H. Meyer, MD
- Paul A. Meyers, MD (Memorial Sloan-Kettering Cancer Center)
- Thomas A. Olson, MD (Aflac Cancer and Blood Disorders Center of Children's Healthcare of Atlanta - Egleston Campus)
- Alberto S. Pappo, MD (St. Jude Children's Research Hospital)
- Arthur Kim Ritchey, MD (Children's Hospital of Pittsburgh of UPMC)
- Carlos Rodriguez-Galindo, MD (St. Jude Children's Research Hospital)
- Stephen J. Shochat, MD (St. Jude Children's Research Hospital)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como "En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]".
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre el tratamiento pediátrico. PDQ Tratamiento del melanoma infantil. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en:
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar
Cláusula sobre el descargo de responsabilidad
Según la solidez de la evidencia, las opciones de tratamiento se clasifican como "estándar" o "en evaluación clínica". Estas clasificaciones no se deben utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del
Última revisión: 2025-01-17
Esta información no reemplaza el consejo de un médico. Ignite Healthwise, LLC, niega toda garantía y responsabilidad por el uso de esta información. El uso que usted haga de esta información implica que usted acepta los
Healthwise, Healthwise para cada decisión de la salud, y el logo de Healthwise son marcas de fábrica de Ignite Healthwise, LLC.
Page Footer
Quiero...
Audiencia
Sitios seguros para miembros
Información sobre The Cigna Group
Aviso legal
Los planes individuales y familiares de seguro médico y dental están asegurados por Cigna Health and Life Insurance Company (CHLIC), Cigna HealthCare of Arizona, Inc., Cigna HealthCare of Illinois, Inc., Cigna HealthCare of Georgia, Inc., Cigna HealthCare of North Carolina, Inc., Cigna HealthCare of South Carolina, Inc. y Cigna HealthCare of Texas, Inc. Los planes de beneficios de salud y de seguro de salud de grupo están asegurados o administrados por CHLIC, Connecticut General Life Insurance Company (CGLIC) o sus afiliadas (puedes ver
Todas las pólizas de seguros y los planes de beneficios de grupo contienen exclusiones y limitaciones. Para conocer la disponibilidad, los costos y detalles completos de la cobertura, comunícate con un agente autorizado o con un representante de ventas de Cigna. Este sitio web no está dirigido a los residentes de New Mexico.